一、事项编码
11652700010283569Y3651072013000
二、适用范围
具有法人资格,或者有独立建制,其负责人应当有法人代表的委托书,能独立公正地开展工作。
三、事项类型
其他行政权力
四、设立依据
1.《医疗器械监督管理条例》(2000年01月04日中华人民共和国国务院令第276号公布;2014年02月12日国务院第39次常务会议修订通过;2014年03月07日中华人民共和国国务院令第650号发布;2017年05月04日公布《国务院关于修改〈医疗器械监督管理条例〉的决定》;2017年05月04日中华人民共和国国务院令第680号发布)
第二十一条:从事第一类医疗器械生产的,由生产企业向所在地设区的市级人民政府食品药品监督管理部门备案并提交其符合本条例第二十条规定条件的证明资料。
2.《医疗器械生产监督管理办法》(国家食品药品监管总局令第37号,2017年修订)
第十一条:开办第一类医疗器械生产企业的,应当向所在地设区的市级食品药品监督管理部门办理第一类医疗器械生产备案,提交备案企业持有的所生产医疗器械的备案凭证复印件和本办法第八条规定的资料(第二项除外)。食品药品监督管理部门应当当场对企业提交资料的完整性进行核对,符合规定条件的予以备案,发给第一类医疗器械生产备案凭证。
五、受理机构
博州市场监督管理局
六、决定机构
博州市场监督管理局
七、办理条件
(一)准予批准的条件
《医疗器械生产监督管理办法》第十一条:开办第一类医疗器械生产企业的,应当向所在地设区的市级食品药品监督管理部门办理第一类医疗器械生产备案,提交备案企业持有的所生产医疗器械的备案凭证复印件和本办法第八条规定的资料(第二项除外)。食品药品监督管理部门应当当场对企业提交资料的完整性进行核对,符合规定条件的予以备案,发给第一类医疗器械生产备案凭证。
(二)不予批准的情形
不符合《医疗器械生产监督管理办法》第十一条的,不予批准
(三)其他需要说明的情形
《医疗器械生产监督管理办法》第二十一条:第一类医疗器械生产备案凭证内容发生变化的,应当变更备案。
备案凭证遗失的,医疗器械生产企业应当及时向原备案部门办理补发手续。
八、申办材料
依据《医疗器械生产监督管理办法》第八条,提交以下资料
序号 |
提交材料名称 |
原件/ 复印件 |
份数 |
纸质/电子 |
1 |
第一类医疗器械生产备案表 |
原件 |
1 |
纸质 |
2 |
企业营业执照复印件 |
复印件 |
1 |
纸质 |
3 |
企业法定代表人或者负责人、质量负责人的身份、学历、职称证明复印件 |
复印件 |
1 |
纸质 |
4 |
企业组织机构与部门设置说明 |
复印件 |
1 |
纸质 |
5 |
企业经营场所、库房地址的地理位置图、平面图(注明实际使用面积)、房屋产权证明文件或者租赁协议(附房屋产权证明文件)复印件 |
复印件 |
1 |
纸质 |
6 |
企业经营设施和设备目录 |
复印件 |
1 |
纸质 |
7 |
企业经营质量管理制度、工作程序等文件目录 |
复印件 |
1 |
纸质 |
8 |
工艺流程图; |
复印件 |
1 |
纸质 |
9 |
所生产医疗器械的备案凭证复印件 |
复印件 |
1 |
纸质 |
10 |
经办人授权证明 |
复印件 |
1 |
纸质 |
11 |
其他证明材料 |
复印件 |
1 |
纸质 |
九、办理方式
网上申报:进入新疆维吾尔自治区医疗器械经营许可系统(http://qxjy.xjfda.com:8087/xzsp_drug/)或新疆政务服务网(http://zwfw.xinjiang.gov.cn/?area=652700)进行网上申报,经博州市场监督管理局网上审核通过后,选择全程电子化登记或半流程电子化登记(网上登记后仍需提交纸质材料)送到博乐市锦绣路6号楼州行政服务中心二楼州市场监管局窗口提交申请。
十、办理流程
(一)流程图:详见附表1
(二)办理程序:依据《医疗器械生产监督管理办法》
第十一条:食品药品监督管理部门应当当场对企业提交资料的完整性进行核对,符合规定条件的予以备案,发给第一类医疗器械生产备案凭证。
包括受理、审核、决定、发证等程序
1.受理阶段:
申请事项属于其职权范围,申请资料齐全、符合法定形式的,应当受理申请。
2.审核阶段:
对申请资料进行审核。
3.决定阶段:
符合规定条件的,依法作出准予许可的书面决定;不符合规定条件的,作出不予许可的书面决定,并说明理由。
4.发证阶段:
作出准予许可决定之日核发《第一类医疗器械生产备案凭证》。
十一、办理时限
(一)法定时限
《医疗器械生产监督管理办法》第十一条:食品药品监督管理部门应当当场对企业提交资料的完整性进行核对,符合规定条件的予以备案,发给第一类医疗器械生产备案凭证。
(二)承诺时限
即办件。
十二、收费依据及标准
(一)收费项目
无
(二)收费依据
无
(三)收费标准
无
十三、结果送达
自受理之日现场取件或电子证书方式送达。
十四、行政救济途径与方式
(一)行政复议
1、部门:博州人民政府
地址:博乐市青得里大街201号
电话:0909-2318444
2、部门:新疆维吾尔自治区市场监督管理局
地址:新疆乌鲁木齐市天山区新华南路167号
电话:0991-2817458
(二)行政诉讼
部门:博乐市人民法院
地址:博乐市南城区锦绣路11号
电话:0909-7688770
十五、咨询方式
(一)现场咨询:博州行政服务中心二楼C区州市场监管局窗口
(二)电话咨询:0909-2271028
(三)网上咨询:http://zwfw.xinjiang.gov.cn/?area=652700
十六、监督投诉渠道
(一)现场监督投诉。博州行政服务中心三楼综合科
(二)电话监督投诉
1.单位投诉电话:0909-2284310
2.博州政务中心投诉电话:0909-2271022
十七、办理地址和时间
地址:博乐市锦绣路6号楼州行政服务中心二楼C区州市场监管局窗口
时间:冬季:上午10:00-14:00,下午15:30-19:30
夏季:上午10:00-14:00,下午16:00-20:00
十八、办理进度和结果查询
1.现场查询:博乐市锦绣路6号楼州行政服务中心二楼C区州市场监管局窗口
2.电话查询:0909-2271028
3.网上查询:http://zwfw.xinjiang.gov.cn/?area=652700
表1
第一类医疗器械生产备案办事流程图
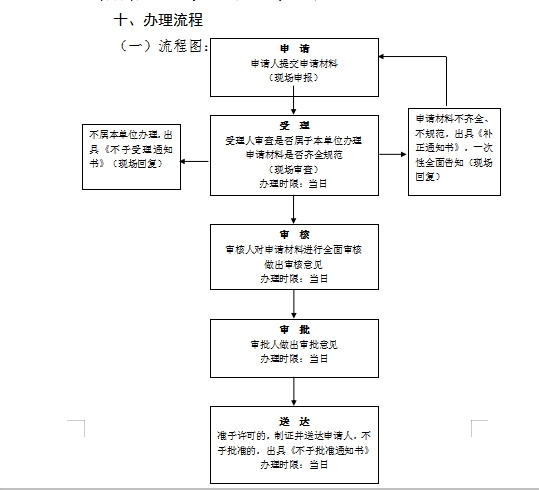
表2
第一类医疗器械生产备案表
企业名称 |
|
统一社会 信用代码 |
|
注册资本 (万元) |
|
成立日期 |
|
营业期限 |
|
企业类型 |
一类 |
|
|
住 所 |
|
邮编 |
|
联系电话 |
|
生产地址 |
|
邮编 |
|
联系电话 |
|
人员情况 |
姓名 |
身份证号 |
职务 |
学历 |
职称 |
法定代表人 |
|
|
|
|
|
企业负责人 |
|
|
|
|
|
联系人 |
姓名 |
身份证号 |
联系电话 |
传真 |
电子邮件 |
|
|
|
|
|
企业人员 情况 |
人员总数(人) |
生产管理人员(人) |
质量管理人员(人) |
专业技术人员(人) |
|
|
|
|
生产场所 情况 |
建筑面积(㎡) |
生产面积(㎡) |
净化面积(㎡) |
检验面积(㎡) |
仓储面积(㎡) |
|
|
|
|
|
检验机构状况 |
总人数 |
|
技术人员数 |
|
备案事项 |
生产范围 |
|
生产产品列表 |
序号 |
产品名称 |
产品备案号 |
备注 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
本企业承诺所提交的全部备案资料真实有效,并承担一切法律责任。同时,保证按照法律法规的要求从事医疗器械生产活动。 法定代表人(签字) (企业盖章) 年 月 日 |
填表说明:1.本表按照实际内容填写,不涉及的可缺项。其中,企业名称、营业执照注册号、住所、法定代表人、注册资本、成立日期、营业期限等按照营业执照内容填写。
2.本表生产范围应当按照国家食品药品监督管理部门发布的第一类医疗器械产品目录和相应体外诊断试剂分类子目录中规定的管理类别、分类编码和名称填写。
常见错误示例
1、经营企业提交的《第一类医疗器械生产备案表》应有法定代表人签字或加盖企业公章;
2、“注册地址”、“库房地址”的填写应明确具体的门牌、楼层和房号。
3、法定代表人的身份证明、学历职称证明、任命文件应有效;
常见问题解答
1.问:一般多长时间可以办完审批手续?
答:即办件。
2.问:收费标准及依据是什么?
答:办理此事项不用收费。
(审核人:杨洪)
 新公网安备 65270102000008号
新公网安备 65270102000008号

